グルコーストランスポーター(英語: glucose transporter、GLUTあるいはSLC2Aと略記)またはグルコース輸送体(グルコースゆそうたい)ないし糖輸送体(とうゆそうたい)は、大部分の哺乳類の細胞に見出される一連の膜タンパクファミリーである。
機能
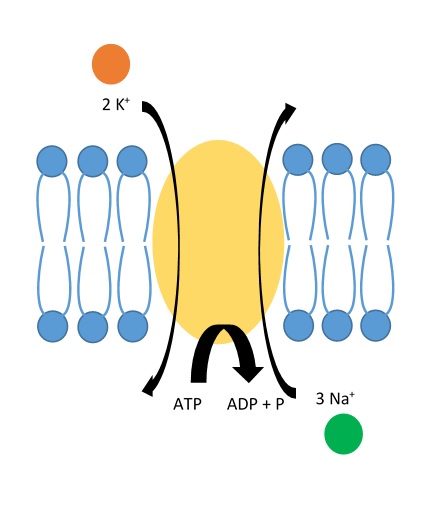
グルコースは、ほとんどの細胞の代謝に不可欠な基質である。グルコースの分子は極性を有するため、生体膜を通過するのには特別な膜輸送タンパク質を必要とする。
能動輸送 - 共役輸送タンパク - SGLT, SLC5A
小腸の頂端膜や腎臓の上皮細胞を通るグルコースの輸送は、ナトリウム-グルコース共輸送体タンパク(後述)のSGLT1およびSGLT2の存在に依存する。SGLTはsodium-dependent glucose transporterまたはsodium/glucose cotransporter の略称である。これらは、ナトリウムポンプのつくるNa の電気化学的勾配によって供給されるエネルギーを利用して二次的に活性化される二次性能動輸送タンパクで、グルコースの細胞内濃度を高める。
腎臓近位尿細管の管腔側に発現しているSGLT2を阻害すると、尿中にろ過された糖の再吸収を抑制し排出を促進するので、糖尿病の治療薬として用いられる。
受動輸送、促進輸送 - GLUT, SLC2A
前述の、細胞膜を通過するグルコースの能動輸送は、輸送促進タンパクのスーパーファミリーのひとつに属するグルコース輸送体(タンパクとしてはGlucose Transporter, GLUT、遺伝子としては溶質キャリヤータンパクファミリー2, Solute Carrier Family 2, SLC2、と表される)によって触媒される。これらの輸送タンパクによって引き起こされる分子の移動は、促進拡散により起こる。このため、能動輸送タンパクがその輸送機構を進行させるのにATPの存在を要求し、ATP/ADP比があまり低下すると立ち往生してしまうのとは異なり、促進拡散輸送タンパクはエネルギーがなくとも機能できる。
構造
GLUTは、12回膜貫通型の膜内在性タンパク質で、アミノ末端とカルボキシル末端の両方が細胞膜の細胞質側に出ている。GLUTタンパクは、交互配座モデルに従いグルコースおよび類似のヘキソースを輸送する。ここから、トランスポーターが基質結合部位を1か所だけ、細胞の外側または内側のいずれかに露出させていることが推論できる。ひとつの結合部位にグルコースが結合すると構造の変化が誘発され、グルコースを輸送して膜の反対側に放出する。内側と外側のグルコース結合部位は、おそらく膜貫通セグメント9、10、11に位置している。また、第7位の膜貫通セグメントに位置するQLSモチーフも、輸送された基質の選択と親和性に関連していると考えられる。
種類
グルコーストランスポーターの各アイソフォームは、グルコースの代謝において、組織発現のパターン、基質特異性、輸送速度論、異なる生理学的状況においての発現調整によって定められた、特色ある役割を果たす。これまでに、14種類のGLUT/SLC2が同定されている。アミノ酸配列の類似性に基づいて、GLUT(グルト)ファミリーは2つのサブクラスに分類されている。
クラスI
クラスIには、目立った特徴を持つグルコーストランスポーターであるGLUT1からGLUT4までが含まれる。
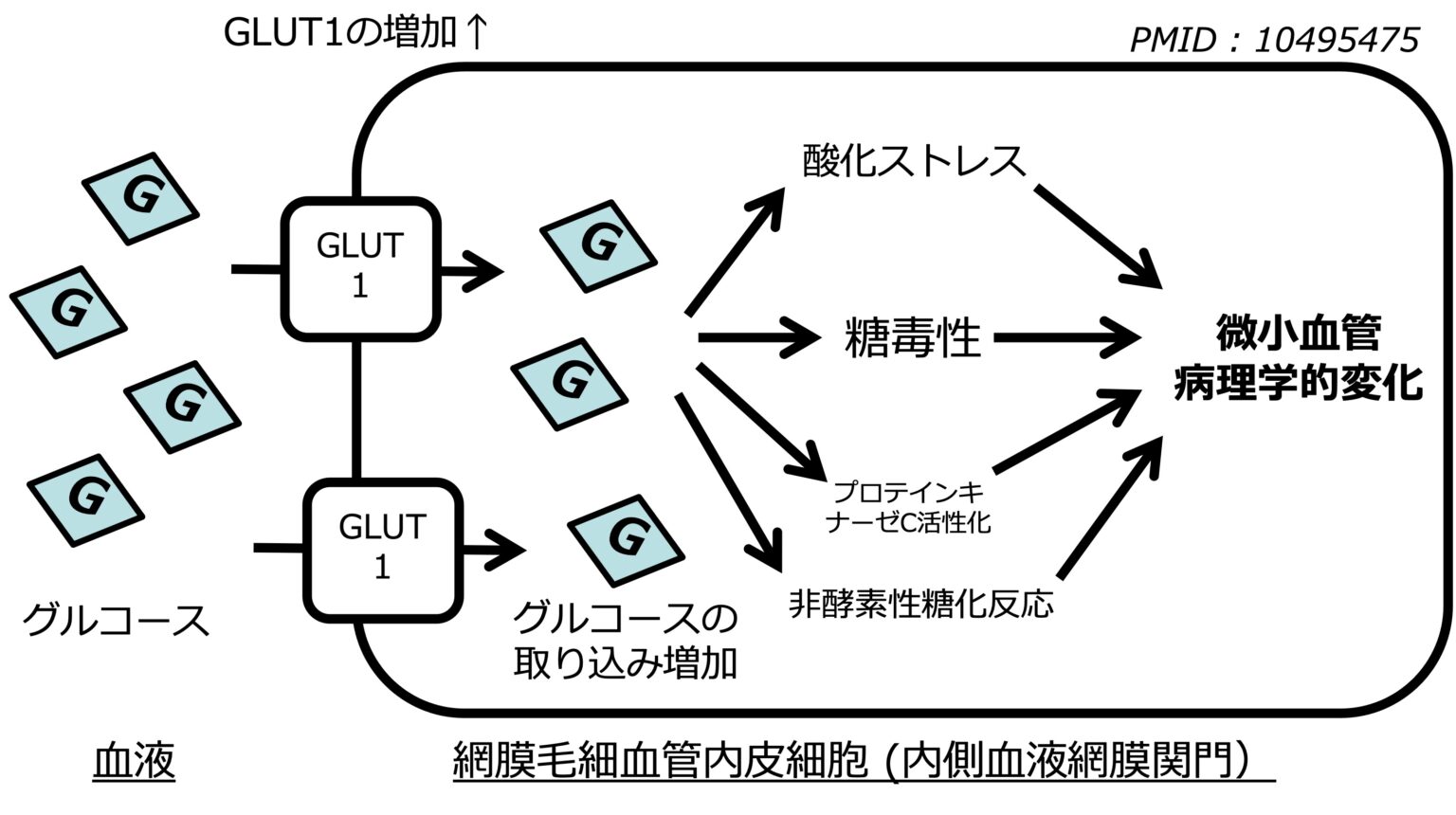
血中のグルコースを脳内に取り込むGLUT1はインスリンでも反応するがインスリンの有無に関わらずGLUT1は細胞膜上に存在してグルコースを取り込む。他方、GLUT4は主に脂肪細胞、骨格筋、心筋に認められ、インスリンがないとき細胞内に沈んでいるが、インスリンにより細胞膜上へと浮上してグルコースを取り込む。脂肪細胞から分泌される分泌蛋白であるアディポネクチンは骨格筋において受容体に結合し、AMPキナーゼを活性化して、通常はインスリンにしか反応しないインスリン感受性のGLUT4を膜の表面へ移動させ、グルコースを細胞内に取り込む作用がある。運動の結果によりアデノシン一リン酸(AMP、アデニル酸)が増加することが知られているが、このAMPがAMPキナーゼを活性化する経路と同じである。つまり、アディポネクチンは、インスリンの作用を介さずに、運動効果とほとんど類似のグルコースを取り込む作用を示すことになる。
クラスII
クラスIIには以下のものが分類される。
- GLUT5 (SLC2A5):フルクトース、グルコースを輸送
- GLUT7 (SLC2A7):小胞体外へグルコースを輸送
- GLUT9 (SLC2A9):フルクトース、尿酸輸送を輸送。近位尿細管に存在。
- GLUT11 (SLC2A11):フルクトース、グルコースを輸送
以前はクラスIIIに分類されていたGLUT6 (SLC2A6)、8 (SLC2A8)、10 (SLC2A10)、12 (SLC2A12) もクラスIIに分類され、主に脳に発現しプロトンとともにイノシトールを輸送するH /myo-イノシトールコトランスポーター (HMIT, SLC2A13)はProton-coupled inositol transporterに分類されている。
クラスIIトランスポーターの大部分は、最近になって、EST (en:Expressed sequence tag)データベースの相同性探査法や、さまざまなゲノムプロジェクトから提供されたアミノ酸配列情報から同定された。
これらの新しく発見されたグルコース輸送体アイソフォームの機能は、現在のところまだ明確には定義されていない。クラスIIトランスポーターは主に細胞内に存在していると考えられていて、このうちのいくつか (GLUT6、GLUT8)は、トランスポーターを細胞内にとどめた結果、グルコース輸送を妨げるような働きを促すモチーフを有している。 これらのトランスポーターの細胞表面への転移を促進する機構が存在するかどうかはまだ不明だが、明確に立証されているのは、インスリンがGLUT6やGLUT8の細胞表面の転移を促進しないということである。
遊離グルコースの合成
ほとんどの細胞では、グルコースの取り込みと異化に関わる唯一の酵素であるグルコース-6-ホスファターゼの発現が欠如しているために、遊離のグルコースを生成することができない。グルコース-6-ホスファターゼを有する肝細胞と、激しい飢餓条件の下での小腸と腎臓のみが、糖新生反応に従って生成したグルコース-6-リン酸のリン酸基を外して遊離のグルコースを生成し、血管中に遊離のグルコースを放出することが可能である。
なお、グルコースが細胞に取り込まれると直ちにリン酸化が起こりグルコース-6-リン酸が生成されるのは、グルコースが細胞膜を超えて拡散してしまうのを防ぐためである。リン酸化により電荷が導入されるので、グルコース-6-リン酸は容易に細胞膜を通過することができない。
ナトリウム-グルコース共輸送タンパク質の発見
1960年4月プラハで、ロバート・K.クレインは、小腸におけるグルコースの吸収機構としてのナトリウム-グルコース共輸送タンパクの発見を初めて発表した。クレインによる同じ方向に送る共輸送体の発見は、生物学上初めて双流対の考え方を提案するものであった。
脚注
関連項目
- シンポート(共輸送)
- 能動輸送
- 受動輸送
- 膜タンパク質
- イオンチャネル
外部リンク
- Glucose Transport Proteins, Facilitative - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)